Anvisa recebe novo pedido para importação de vacina Covaxin
Solicitação foi feita pelo Ministério da Saúde. Objetivo é importar 20 milhões de doses
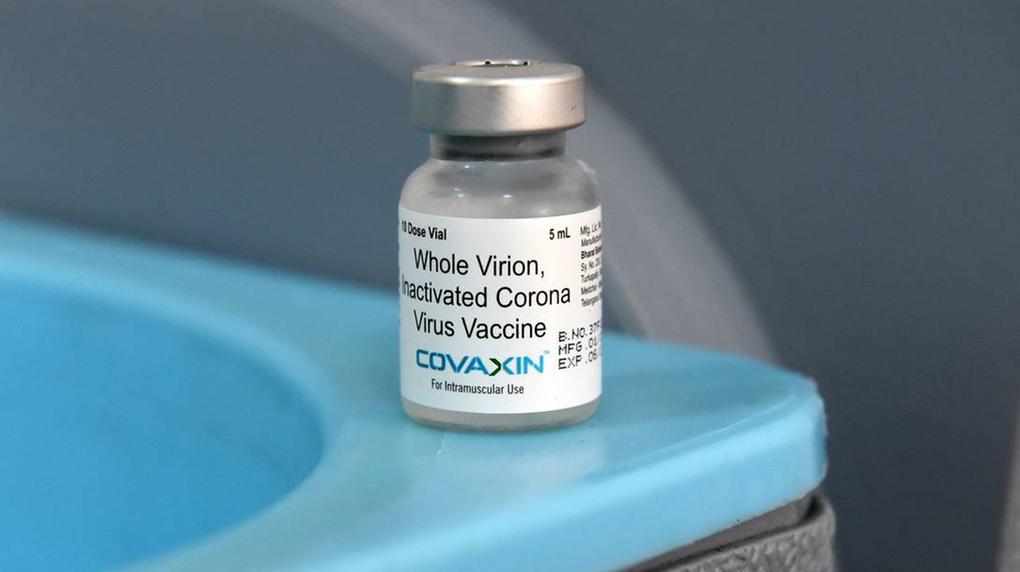
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu, nesta segunda-feira (24), um novo pedido de autorização do Ministério da Saúde para importar 20 milhões de doses da vacina Covaxin. O imunizante para a Covid-19 é fabricado pela empresa indiana Bharat Biotech.
Essa será a segunda tentativa do Ministério de obter aval para importar a vacina. Um primeiro pedido foi feito em março, mas foi negado pela agência por falta de documentos e de certificado de boas práticas de fabricação pela empresa.
Veja também
Segundo a Anvisa, após a negativa do primeiro pedido, o Ministério da Saúde e a Precisa Medicamentos, laboratório brasileiro que mantém uma parceria com a Bharat Biotech, seguiram em tratativas com a agência para "adequar os aspectos que motivaram o indeferimento".
Recentemente, a agência deu aval para um pedido de realização de estudo clínico, no Brasil, da vacina Covaxin. A previsão é que os testes envolvam até 4,5 mil voluntários nos estados de São Paulo, Rio de Janeiro, Bahia e Mato Grosso, e sirvam como complemento a dados obtidos em estudo feito na Índia.
Análise do novo pedido
A farmacêutica, porém, ainda precisa ajustar pontos que levaram à negativa anterior da análise de boas práticas de fabricação.
"No que se refere ao cumprimento das Boas Práticas de Fabricação pela fabricante Bharat Biotech, um dos principais aspectos que motivou a decisão anterior, a empresa protocolou novo pedido de certificação na Anvisa, referente à linha de produção do produto acabado", informa a agência, em nota.
Ainda segundo a Anvisa, o novo pedido de importação foi protocolado com base na lei 14.124/2021. A medida abre espaço para que Anvisa faça a análise de uma possível autorização excepcional a vacinas sem registro ou uso emergencial no Brasil, mas aprovadas em alguns outros países - entre eles, a Índia, onde a aprovação da Covaxin ocorreu antes do fim dos testes clínicos.
A previsão é que o pedido seja analisado em até sete dias úteis. O prazo, no entanto, pode ser suspenso em caso de falta de documentos.






.jpg?f=4x3&h=216&w=288&$p$f$h$w=3e133aa)


.jpeg?f=4x3&h=216&w=288&$p$f$h$w=51aa9b6)



.jpg?f=4x3&h=216&w=288&$p$f$h$w=60627be)




